Время прочтения - 3 мин.
Американское агентство выдало первое согласие регулирующих органов на использование препарата Ремдесивир от Gilead в качестве лекарства от COVID-19. Препарат уже применялся в терапии некоторых пациентов, включая Дональда Трампа.
Первый пошел
Компания Gilead первой получила одобрение регуляторных органов США после того, как FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов) одобрило ее противовирусный Ремдесивир для пациентов, госпитализированных с коронавирусом.
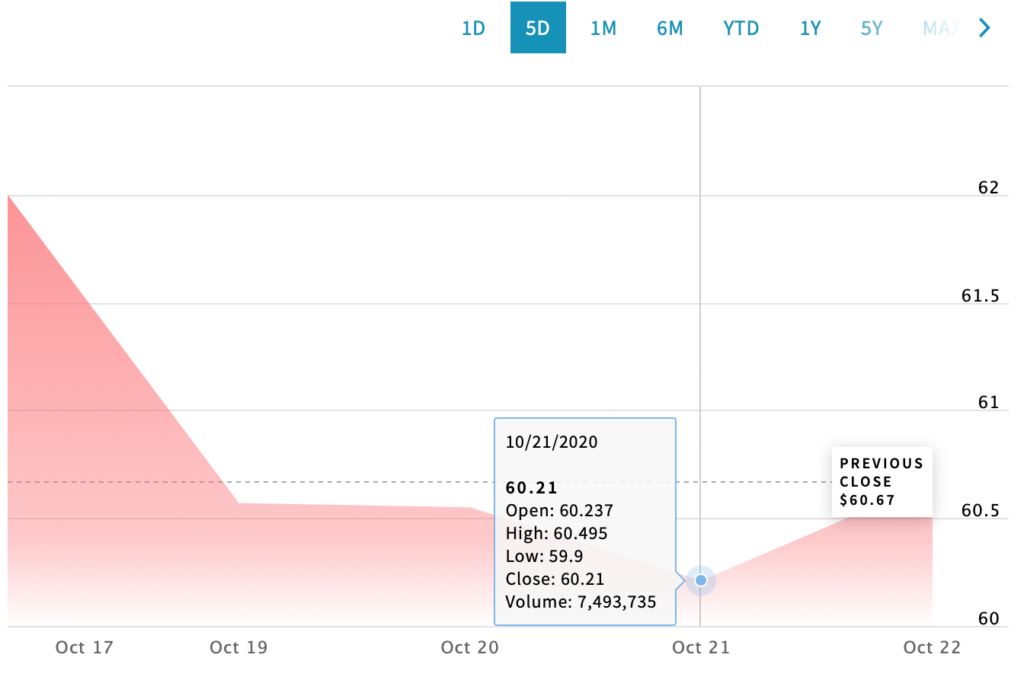
Акции Gilead
Акции Gilead выросли на 4,2% (до $63,18) на закрытии торгов после заявления FDA. Ремдесивир, ныне известный под торговой маркой Veklury, изначально разработан для лечения лихорадки Эбола.
Противовирусное средство уже использовалось для лечения пациентов в экстренных случаях. Именно этот препарат стал одним из тех, что получал президент США Дональд Трамп, подхватив COVID-19.
Ускоряет, но не спасает
Клинические испытания показали, что Ремдесивир способен ускорять выздоровление, но мало влияет на вероятность выживания пациентов.
Дэниел О’Дей, исполнительный директор, говорит, что Gilead «неустанно» работал над поиском решений для борьбы с пандемией.
«Скорость и строгость, с которой Veklury был разработан и одобрен в США, отражают общую приверженность Gilead, государственных учреждений и исследователей клинических испытаний задаче создания эффективных вариантов лечения COVID-19», — говорит он.
Компания Gilead значительно расширила выпуск препарата, чтобы удовлетворить спрос на Ремдесивир, который уже используется в качестве стандартного варианта терапии от коронавируса в США. Недавно компания подписала договор с Европейской комиссией на сумму €1 млрд на поставку 500 000 курсов лечения.
На прошлой неделе компания Gilead пережила неудачный момент, когда испытание Всемирной организации здравоохранения «Solidarity» показало, что препарат мало влияет на снижение показателей смертности. Но при этом он сокращает время пребывания в клинике и необходимость в искусственной вентиляции легких. В исследование свойств Ремдесивира было задействовано 2 750 пациентов.
Впервые Gilead предоставила препарат на одобрение в августе, еще до того, как стали известны результаты испытаний Solidarity.
Кто может использовать препарат?
Лекарство предназначено для взрослых и детей старше 12 лет, находящихся на стационарном лечении, но не подключенных к ИВЛ. Препарат вводят внутривенно в течение пяти дней. Gilead также сообщила, что получила разрешение на применение Ремдесивира — в экстренных случаях — для детей до 12 лет или с массой тела менее 40 кг.
Барри Зингман, профессор медицины, курировавший испытание Ремдесивира в Медицинском центре Монтефиоре в Нью-Йорке, считает, что одобрение FDA стало «важной вехой», которая поможет улучшить результаты лечения пациентов и сохранить ресурсы здравоохранения.
Источник: CNBC, FT
Подпишись на наш телеграм канал
только самое важное и интересное










